Biosimilares: la vía rápida para universalizar los tratamientos más punteros
El primer informe que analiza la penetración de estos medicamentos en la sanidad pública revela grandes diferencias entre comunidades
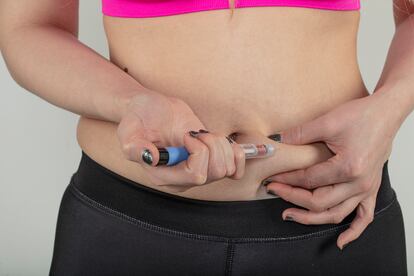

El mayor éxito comercial de la historia de la industria farmacéutica se llama Humira. Este anticuerpo monoclonal, indicado para múltiples procesos autoinmunes e inflamatorios como la artritis reumatoide, ha proporcionado a la compañía estadounidense Abbvie unos ingresos superiores a los 200.000 millones de euros desde 2002. El elevado precio de los medicamentos innovadores —más de mil euros al mes por paciente en España, en este caso— obliga a los sistemas sanitarios a ser cautos a la hora de universalizar su uso.
“Las guías clínicas ordenan las opciones de tratamiento, según su balance coste-beneficio, porque es la forma de dar el mejor uso a los recursos disponibles. Los nuevos fármacos biológicos como el adalimumab [el principio activo del Humira] tienen precios tan elevados que suelen ponerse en tercera línea. Esto supone que el paciente deberá tomar primero dos tratamientos y, solo si estos fracasan, recibirá el puntero.”, explica Encarna Cruz, directora general de la Asociación Española de Medicamentos Biosimilares (BioSim). Esta situación cambia sustancialmente si, al expirar las patentes, entran en escena los medicamentos biosimilares. “Al tener un precio mucho menor [hasta el 80%], no solo ahorran recursos al sistema, sino que también pueden ayudar a que más pacientes reciban estas terapias”, añade.
BioSim ha presentado este martes en Madrid el primer informe completo sobre la penetración de los biosimilares en la sanidad pública. Titulado Estudio sobre el mercado de medicamentos biosimilares en el Sistema Nacional de Salud en España, el trabajo ha sido coordinado por Jaime Espín, profesor de la Escuela Andaluza de Salud Pública y exasesor del Banco Mundial y la Comisión Europea. La principal conclusión es que existe “una gran heterogeneidad en todos los aspectos del mercado de los biosimilares”, según el autor.
Si se mira a los hospitales, por ejemplo, en los medicamentos en los que existe una versión biosimilar, la cuota de mercado de estos fármacos asciende al 73% de media, mientras este porcentaje desciende al 30% entre los de venta en las farmacias. Las diferencias son también enormes entre comunidades autónomas. País Vasco es la que menor penetración de biosimilares tiene (31%), mientras Castilla-La Mancha tiene casi el doble (54%). La media nacional es del 46%. Las cifras son igualmente muy dispares según los tipos de medicamentos o las enfermedades para la que están indicados.
“España tiene un amplio margen de mejora”, ha defendido Espín en referencia a la incorporación de biosimilares en el sistema sanitario. Según el estudio, el país ocupa una posición intermedia en Europa, donde los países nórdicos ocupan las posiciones de cabeza y los del este del continente una posición más rezagada. Este experto ha defendido que el beneficio más importante que conlleva una mayor penetración de los biosimilares no es el ahorro, sino que con ellos se “mejora la eficiencia” y los tratamientos punteros “llegan a más pacientes”. Con este objetivo, y dada la variabilidad existente en Espala, es son necesarias “políticas que den un impulso” a este tipo de fármacos.
Un dato importante a destacar es que las diferencias de penetración de los biosimilares (al igual que los genéricos) entre comunidades no suponen que haya diferencias de acceso de los pacientes a los tratamientos según donde vivan. En España, el sistema de precios de referencia hace que todos los fármacos equivalentes (el de marca y el biosimilar) deban tener el mismo coste para el sistema sanitario. Menos presión de la competencia de biosimilares y genéricos, por tanto, supone una menor presión para que desciendan los precios y, por tanto, mejore la eficiencia del sistema, pero no abre la puerta a inequidades.
Las moléculas de los medicamentos biológicos —hormonas como la insulina, anticuerpos...— suelen ser muy grandes, con largas y complejas cadenas de más de 20.000 átomos. Unas dimensiones que contrastan con las pequeñas y sencillas estructuras de los fármacos de síntesis química (de unos 120 átomos máximo). Esto hace que, a diferencia de los medicamentos genéricos, que pueden copiar al detalle los fármacos de síntesis química, los biosimilares tengan pequeñas diferencias con el original, sin que esto afecte a su calidad, eficacia y seguridad.
“Aunque tengan diferencias en cuestiones de desarrollo y regulatorios, biosimilares y genéricos coinciden en que promueven la competencia en el mercado, consiguen una reducción de precios en el sistema y mejoran su eficiencia”, destaca Espín.
Las conclusiones del estudio abogan por la conveniencia de crear un Observatorio de Biosimilares que, al igual que la elaboración de esta primera edición del trabajo, requieren una mayor transparencia y disponibilidad de los datos del Sistema Nacional de Salud. “Lo que no se mide no se puede mejorar, y lo que no se mejora se degrada”, afirma Espín.
El director general de Farmacia del Ministerio de Sanidad, César Hernández, ha expresado en el acto de presentación del informe que la voluntad del departamento es ser “la fuente primaria de información sobre los medicamentos biosimilares” y que los datos deberían estar a disposición del público de la manera “más actualizada posible”.
Hernández también se ha mostrado partidario del fomento de los biosimilares y ha apuntado a la actual legislación sobre los precios de referencia –que iguala el de los fármacos originales con el de los biosimilares y también los genéricos—como una de las barreras, ya que “no fomentan la competencia”.
La subdirectora de BioSim, Isabel del Río, ha destacado en el acto otro beneficio potencial del Observatorio: la posibilidad de disponer de información sobre las políticas más relevantes llevadas a cabo en España por las comunidades para el fomento de los biosimilares.
Félix Lobo, presidente del Comité Asesor para la Prestación Farmacéutica (CAPF) y profesor emérito de la Universidad Carlos III de Madrid, ha manifestado por su parte que es “de esperar y hasta deseable” que haya diferencias entre los datos de las distintas comunidades autónomas, ya que esto permite “identificar” las mejores prácticas de gestión y extenderlas al resto. Pero para hacerlo “debe haber transparencia ya que solo disponer de datos y buenos indicadores es un avance” y, por otro lado, se debe profundizar en evaluación de tecnologías y servicios, así como “poner el punto de mira en los resultados en salud”.
Sobre la firma