Medicamentos probados en blancos que no sirven para negros
La mayoría de los fármacos se ensayan en población de origen europeo, pero sus recomendaciones de uso y dosificación se exportan a África y otros lugares del mundo. Las poblaciones subsaharianas, genéticamente muy diversas, sufren las consecuencias de ingerir medicamentos a ciegas

El efavirenz es un antirretroviral de uso común que ha contribuido a salvar millones de vidas en África subsahariana. Y ha provocado, por el camino, graves cuadros psiquiátricos: depresión, paranoia, ideaciones suicidas... Hoy se sabe que los africanos negros son genéticamente más propensos a sufrir estos efectos adversos. Son complicaciones que también se dan entre enfermos de sida con origen europeo o asiático, aunque en mucha menor medida.
La explicación proviene de cierta variante africana en la encima CYP2B6, relacionada con el metabolismo del efavirenz. Esta se encuentra en la mitad de la población subsahariana. Su presencia conlleva una lenta absorción y eliminación del antirretroviral, lo que hace que aumente la toxicidad y dispare la posibilidad de daño psiquiátrico.
Para sortear el riesgo, una opción pasa por reducir la dosis. Ante una alta probabilidad de metabolismo lento, se administra menos principio activo. Otra es decantarse por antirretrovirales en teoría más seguros como el dolutegravir. Así hicieron en 2019 —siguiendo las recomendaciones de la Organización Mundial de la Salud— países como Botsuana y Sudáfrica.
Nicola Mulder, profesora de biología computacional en la Universidad de Ciudad del Cabo (Sudáfrica), recurre al ejemplo del efavirenz para ilustrar cuánto importa, al ingerir medicamentos, el factor étnico. “Las diferencias genéticas entre poblaciones pueden tener un enorme impacto en los tratamientos, suponiendo a veces problemas significativos de salud”, apunta. “Lo que sirve para los europeos no es necesariamente lo que sirve para los africanos”, añade, más explícita, Ann Daly, profesora de farmacogenética en la Universidad de Newcastle (Reino Unido).
Acuñada por el alemán Friedrich Vogel en 1959, la farmacogenética admite distintas definiciones. Leves sutilezas que giran en torno a una obviedad: los humanos respondemos de forma diferente al mismo fármaco. En buena medida, por rasgos inmutables, sellos genéticos que, incrustados como están en nuestro ADN, nos acompañan de por vida.
En África están entrando millones de medicamentos y no tenemos ni idea de qué puede ocurrir. Quizá en el futuro nos encontremos con serios problemas de salud públicaPedro Gil, Karolinska Institutet de Estocolmo
“En África están entrando millones de medicamentos y no tenemos ni idea de qué puede ocurrir. Quizá en el futuro nos encontremos con serios problemas de salud pública”, alerta Pedro Gil, investigador portugués del Karolinska Institutet de Estocolmo (Suecia). Si Occidente cuenta con advertencias a priori (sustentadas en horas de laboratorio), en África empiezan a saltar alarmas a posteriori. Así ha ocurrido con el efavirenz y su alta incidencia, al sur del Sáhara, de efectos nocivos sobre la salud mental.
Gil explica cómo algunos programas contra la malaria también están cosechando los frutos de la ignorancia. Cuenta que la amodiaquina (un fármaco profiláctico muy usado contra el paludismo estacional en el Sahel) provoca, en países como Mali, fuertes molestias estomacales a un 30% de los niños. Se sabe que la raíz del problema es, de nuevo, genética. El dolor de tripa hace que “muchas madres dejen de dar la pastilla a sus hijos”, continúa Gil. No solo se está perdiendo la confianza en este medicamento, sino quizá ante “futuros tratamientos”, lamenta.
A nivel individual, la farmacogenética permite vislumbrar tratamientos de precisión y adaptados a las características del paciente. Abre la puerta a que los médicos elijan y dosifiquen fármacos con una óptica microscópica, sin casi margen de error.
Por el contrario, cuando se aborda desde una perspectiva étnica, poblacional, la farmacogenética solo aspira a concluir promedios. Da información valiosa sobre la respuesta probable (aunque no segura) de un paciente dependiendo de su etnicidad. Se aleja así del ideal de una medicina rigurosamente personalizada. Pero, a cambio, sostienen sus defensores, permite afinar el tiro en la distribución de fármacos a escala masiva. Sobre todo, cuando no resulta viable hacer un test genético a cada paciente.
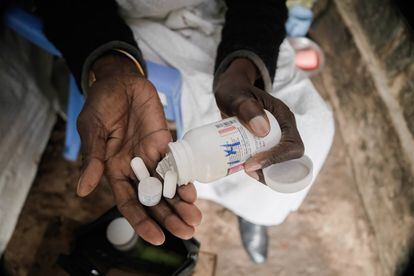
Los pacientes con ancestría subsahariana se enfrentan a una doble negligencia. Tienen un peso ínfimo en los ensayos clínicos previos al lanzamiento de un nuevo fármaco y escasean en las muestras que nutren la prolífica investigación farmacogenética de las últimas décadas. Un metaanálisis (estudio de varios estudios) desgranó en 2020 cientos de publicaciones sobre posibles correlaciones genéticas en 300 fármacos. Solo en 15 medicamentos figuraban —en las cohortes estudiadas— representantes de origen africano. Casi la mitad eran descendientes de esclavos en EE UU.
Carentes de información contrastada, los subsaharianos toman medicinas casi a ciegas. Han de confiar en que la respuesta prevista en poblaciones caucásicas (y, en menor medida, asiáticas) se aplique también en su caso. Deben, en última instancia, conformarse con las recomendaciones dictadas desde los laboratorios y centros de investigación occidentales.
Desde la Universidad de Port Harcourt, en Nigeria, la psiquiatra e investigadora Frances Adiukwu narra idénticos peligros. Afirma estar obligada a utilizar el “ensayo y error” sobre el terreno, a pie de consulta. Subraya lo mucho que cuesta en su país que individuos con patologías graves (esquizofrenia, trastorno bipolar) acudan al psiquiatra. “Suelen ir antes al curandero o al pastor. Cuando al fin vienen, si estamos cambiando la dosis o el fármaco continuamente, pierden fe en el sistema”, comenta.
Y las enfermedades, continúa, “empeoran, lo que redunda negativamente en el bienestar del paciente, que es el fin último de la medicina de precisión”. Adiukwu plantea una hipótesis para ejemplificar su argumento: “Quizá el 60% de la gente del norte de Nigeria sea metabolizadora rápida. Lo lógico sería entonces empezar los tratamientos con dosis altas”.
En Europa hay poca diversidad genética y mucho dinero; en África hay poco dinero y mucha diversidadInnocent Assimwe, investigador de la Universidad de Liverpool
El pasado año, Adiukwu rastreó la literatura científica sobre farmacogenética en el campo de la psiquiatría. Su búsqueda arrojó 2.550 resultados entre los años 2020 y 2022. Menos de 40 mencionaban a las poblaciones africanas. Soliviantada, contactó con las máximas autoridades en la materia para intentar mitigar tamaño vacío. No obtuvo respuesta, así que envió un artículo a The Lancet, la biblia de las revistas médicas. “Sentí que debía hacer algo, poner mi granito de arena”, asegura.
En seguridad y eficacia farmacológica, la desventaja del África Subsahariana arrastra otro punto flaco: la inmensa riqueza genética de esta región. “Solo en un país como Gabón hay más diversidad que en toda la Unión Europea. Quizá portugueses y finlandeses tengamos un aspecto muy diferente, pero farmacogenéticamente somos casi clones”, asevera Gil.
Innocent Assimwe, investigador en el centro de medicina personalizada de la Universidad de Liverpool, natural de Uganda, resume las causas de la desigualdad intercontinental en la exposición a fármacos: “En Europa hay poca diversidad y mucho dinero; en África hay poco dinero y mucha diversidad”.
La conclusión se antoja obvia. Donde más habría que investigar las diferencias étnicas en la respuesta a medicamentos, menos se hace. Y, sin embargo, la profunda asimetría de medios y el status quo en la industria farmacéutica mantienen, en opinión de Assimwe, la inercia de un mantra con cierto regusto colonial: “Si un fármaco es seguro para los blancos, es seguro para los negros”.
Assimwe ha analizado a fondo el componente étnico en los estudios sobre el warfarin, el anticoagulante más utilizado en el mundo. Sus resultados confirman el patrón de sesgo caucásico. Las evidencias que se desprenden de las investigaciones son de utilidad para los pacientes de origen europeo. Y, hasta cierto punto, de algunas regiones de Asia. Pero no sirven demasiado para aquellos con ancestros africanos o las poblaciones indígenas de Latinoamérica.
El equipamiento para realizar PCR sirve también para hacer test genéticos. Quizá un muy aprovechable efecto secundario de la pandemia para genotipificar al crisol étnico subsahariano
Gil apuesta por proyectar un sólido rayo de luz ante tanta oscuridad. Pasaría por genotipificar al crisol étnico subsahariano, poniendo el foco en las variantes que más influyen en el metabolismo de fármacos. Dice el investigador portugués que tan ambiciosa empresa ya no es un sueño inalcanzable. La covid-19 lo ha hecho posible. “La transferencia de tecnología de los últimos años representa una increíble oportunidad”, asegura. Al parecer, el equipamiento para realizar PCR sirve también para hacer test genéticos. Un guiño del destino. O quizá un muy aprovechable efecto secundario de la pandemia.
Aunque Assimwe admite que esto supondría un avance notable, también recuerda las limitaciones de las máquinas para hacer PCR. “Son capaces de genotipificar de acuerdo a ciertas variantes, pero no de descubrir otras nuevas que quizá sean las que importan en la respuesta de las poblaciones negras a fármacos como el warfarin”, asevera. La infraestructura que permite zambullirse de lleno en los laberintos del genoma humano (con sus complejos puzzles de polimorfismos, alelos y otros tecnicismos) “resulta mucho más cara”, destaca Assimwe.
El proyecto H3Africa nació precisamente con ambos objetivos —genotipificar a las poblaciones del continente mientras se buscan nuevas variantes— entre sus máximas prioridades. Creado en 2010 gracias a donantes británicos y estadounidenses, el proyecto ha permitido tejer una red investigadora con una misión común: angostar la brecha que aleja a África de la revolución genético-sanitaria global. Entre sus logros, destaca haber genotipificado a unos 50.000 africanos de 30 países. Una cifra aún modesta frente a la abrumadora heterogeneidad de ADN que circula por el continente.
Si nada lo remedia, H3Africa como tal morirá en breve. El período de financiación está a punto de expirar. No hay visos de prórroga. La profesora Mulder, de la Universidad de Ciudad del Cabo, ha estado coordinando la división bioinformática del proyecto. Confía en que, cuando se corte definitivamente el grifo de fondos, sus participantes den con la fórmula que permita algún tipo de continuidad: “Barajamos varias opciones, entre ellas convertirnos en una ONG”. Todo con el objetivo de que “algunas actividades conjuntas sigan su marcha”.
Puedes seguir a PLANETA FUTURO en Twitter, Facebook e Instagram, y suscribirte aquí a nuestra ‘newsletter’.
/cloudfront-eu-central-1.images.arcpublishing.com/prisa/W6HIBKZDWRHUPIFPOHKIOW4CAU.jpg)